Estudio Comparativo de “SEROPERFILES”.
Luna A. Miguel Angel
CENID-Microbiología Animal INIFAP.
[email protected]
[email protected]
Oliveros IJM Asesor Clínica Privada.
Morales AJJ Asesor Clínica Privada.
Socci EG CENID-Microbiología Animal INIFAP.
Banda RV CENID-Microbiología Animal INIFAP.
Luna REM Depto. De Biomedicina Molecular CINVESTAV.
RESUMEN

La leptospirosis es una enfermedad de origen bacteriano de los animales que puede afectar accidentalmente al hombre. Es causada por diversos microorganismos con forma helicoidal del género Leptospira especie interrogans. La bacteria puede entrar al organismo a través de mucosas, piel lacerada o reblandecida y ser eliminada a través de la orina y secreciones postaborto de animales infectados diseminando la infección.
En caprinos existe poca información al respecto, la literatura se limita a mencionar la similitud que existe con la leptospirosis bovina y ovina, así como a reportar esta especie como una de las más resistentes a la infección. Con el fin de conocer el estatus de la enfermedad en caprinos se realizó un estudio serológico de la leptospirosis en dos unidades de producción caprina con antecedentes de trastornos reproductivos y sin medidas de control de vacunación contra la enfermedad. Ambas unidades se especializan en la producción de leche y se encuentran localizadas en el municipio de Apaseo El Alto, Guanajuato. Para realizar la detección de anticuerpos contra Leptospira se utilizó la prueba de aglutinación microscópica “MAT” propuesta por la Organización Mundial de Sanidad Animal (OIE) y la Organización Mundial de la Salud (WHO). Los animales que reaccionaron con títulos mayores o iguales a 1:100 fueron considerados como positivos.
Las unidades de producción se denominaron “A” y “B”. De un total de 60 muestras de la unidad“A”el68.3%(41/60)resultaronpositivas, con títulos que oscilaron de 1:100 a 1:1,600; las serovariedades más frecuentes fueron: Icterohaemorrhagiae cepa Palo Alto (aislado nacional); Canicola serovariedad Portland-vere (aislado nacional); Hardjo cepa H-89 (aislado nacional) y Grippotyphosa. De un total de 134 muestras de la unidad “B”el 72.4% (97/134) mostró positividad, con títulos que oscilaron de 1:100 a 1:800.

Las serovariedades más frecuentes fueron: Bratislava, Icterohaemorrhagiae cepa Palo Alto (aislado nacional), Canicola serovariedad Portland-vere (aislado nacional) y Grippotiphosa. Las frecuencias de anticuerpos reportadas por etapa variaron entre la unidad “A” y “B” de un 20% para cabritos a un 100% para animales adultos. Se concluye que los anticuerpos detectados por la prueba de “MAT” en el presente estudio fueron generados por un proceso infeccioso, dado que los animales nunca fueron vacunados contra la leptospirosis, así como la necesidad de implementar un programa de vacunación contra la enfermedad con un biológico que contenga las serovariedades de Leptospira identificadas para lograr un adecuado control de la enfermedad.
INTRODUCCIÓN
La leptospirosis es una enfermedad bacteriana infectocontagiosa de los animales y el hombre causada por diversos microorganismos de forma helicoidal del género Leptospira especie interrogans (Fig. 1). La infección es trasmitida a través de la orina y las secreciones post-aborto de animales infectados, y es capaz de ingresar al organismo a través de mucosas y piel lacerada o reblandecida por contacto con el agua. Los signos clínicos pueden ser graves, leves o inaparentes y el curso agudo o crónico. La recuperación generalmente se asocia con la aparición de anticuerpos específicos contra la enfermedad y un estado de portador de la bacteria a nivel renal eliminando el microorganismo a través de la orina durante meses o años.
La leptospirosis presenta una frecuencia estacional incrementándose durante la época de lluvias, así como en desastres naturales: huracanes o inundaciones. Todas las especies de animales domésticos y silvestres así como el hombre son susceptibles a la infección. En el ser humano es capaz de ocasionar trastornos febriles, hepático-renales, neumonías, hemorragias pulmonares, hemoptisis, trastornos circulatorios, insuficiencia cardiaca y muerte (Fig. 2).
Motivo por el cual en el año 1999 la Secretaria de Salubridad y Asistencia generó una serie de estrategias para su control a través de la norma oficial mexicana NOM-029-SSA2-1999, y en años recientes el mismo órgano institucional generó un proyecto de vigilancia epidemiológica para esta enfermedad PROY- NOM-017-SSA-2012. El impacto de la leptospirosis en especies animales tales como el ganado bovino también se ha reflejado en la generación de estrategias para su control descritas en la norma NOM-038-ZOO-1995. Sin embargo en pequeños rumiantes y específicamente en caprinos no sólo se carece de normas o estrategias preventivas para su control, sino se desconoce la importancia y el papel que juega la cabra como reservorio y transmisor de la enfermedad a otras especies, incluyendo al hombre. El presente estudio tiene como objetivo ampliar la información sobre la leptospirosis caprina y resaltar su importancia en la ganadería nacional.
|
Cuadro 1. Manifestaciones clínicas, trastornos y lesiones presentes en la leptospirosis caprina. |
|||
|
Presentación Aguda |
Presentación crónica |
Trastornos |
Lesiones |
|
Fiebre |
Abortos |
Renales |
Petequias |
|
Depresión |
Partos prematuros |
Reproductivos |
Equimosis |
|
Anorexia |
Mortalidad Neonatal |
Hepáticos |
Sufusiones |
|
Ictericia |
Mortalidad Perinatal |
Musculares |
Nefritis |
|
Hemoglobinuria |
Infertilidad, reabsorciones |
Nerviosos |
Nefrosis |
|
Anemia |
Baja concepción |
Pulmonares |
Hepatitis |
|
Emaciación |
Repetición de estros |
||
|
Muerte |
Baja producción de leche |
||
| Manual Merck de Veterinaria 1988; Lilenbaum 2007; Hatem, 2014. | |||
ANTECEDENTES.

La leptospirosis caprina se ha reportado en países alrededor de todo el mundo. Sin embargo, la literatura se limita a mencionar que la enfermedad clínica y las lesiones se “asemejan” a la leptospirosis en bovinos y ovinos, por lo que mucha información publicada en esta especie se fundamenta en esta primicia. Así mismo, se reporta a los caprinos como la especie menos susceptible a la leptospirosis, considerándola de poca importancia (Manual Merck, 1981; Faine, 1982; Hagan y Bruner, 1983).
Otros autores consideran a la leptospirosis caprina como una enfermedad que causa un “fuerte impacto” en los trastornos reproductivos y productivos de las cabras, lo que ocasiona una disminución de la fertilidad, mortalidad neonatal, abortos y disminución de la producción de leche trayendo como consecuencia pérdidas económicas (Lilenbaum, 2007). La importancia de estos trastornos se exacerban por las características epidemiológica de la leptospirosis, a la cual se considera como una enfermedad de “poblaciones” (rebaños o hatos) y no individual (Hernández, 2005).

La enfermedad se puede manifestar en forma aguda en animales jóvenes y suele ser mortal. La forma crónica se da en animales adultos, en los que ocasiona trastornos reproductivos. Hatem (2014) reporta en Egipto un brote agudo en ovinos caracterizado por fiebre, ictericia, hemoglobinuria, aborto y muerte de animales afectados. La forma crónica es más frecuente y se caracteriza por aborto, mortinatos, muerte perinatal, infertilidad y ocasiona en los animales el estado de portador de la bacteria a nivel renal (Cuadro 1). Debido a que estas manifestaciones clínicas también suelen presentarse en otras enfermedades reproductivas la leptospirosis puede pasar desapercibida por los productores al atribuir estos trastornos a otras enfermedades infecciosas como brucelosis o clamydiasis.
Al igual que otras enfermedades reproductivas la infección puede permanecer latente hasta la gestación. En esta etapa la bacteria atraviesa la barrera placentaria, infecta al feto y puede ocasionar lesiones multiorgánicas, muerte y aborto del producto o bien el animal nace infectado y muere a los pocos días. Las lesiones en placenta son poco definidas o claras ya que la bacteria afecta principalmente al producto (http://www.capraispana.com/enfermedades/ aborto/aborto.htm).
El diagnóstico de la enfermedad se realiza por estudios
directos e indirectos. Los estudios directos involucran: 1. Observación del microorganismo al microscopio de campo oscuro. 2. Aislamiento bacteriano, el cual en la mayoría de los casos resulta infructuoso y poco práctico. 3. Métodos moleculares como la reacción en cadena de la polimerasa (PCR). Las técnicas indirectas abarcan todas las técnicas serológicas utilizadas para la detección de anticuerpos como el inmunoensayo o “ELISA” y la técnica de aglutinación microscópica o “MAT” con antígeno vivo considerada como la prueba de “oro” en el diagnóstico de la leptospirosis.
Un perfil serológico o seroperfil es un muestreo sanguíneo que tiene como objetivo obtener el suero de un grupo de animales de diferentes edades y etapas reproductivas para identificar por técnicas de laboratorio la presencia de anticuerpos para una enfermedad determinada. Los perfiles serológicos permiten determinar el estado y la situación sanitaria de una población animal (rebaño, hato) y analizar su respuesta inmune con respecto a la enfermedad de interés y poder así, tomar las medidas de control más adecuadas (manejo, vacunación o tratamiento de animales afectados) (Morilla, 1997).
|
Cuadro 2. Serovariedades de Referencia Internacional y de Aislamiento Nacional Utilizados Como Antígenos para el Diagnóstico de Leptospirosis en la Prueba de “MAT”. |
|||
|
Genomoespecie |
Serogrupo |
Serovariedad |
Cepa |
|
L. interrogans |
Icterohaemorrhagiae |
Icterohaemorrhagiae |
RGA |
|
L. interrogans |
Pyrogenes |
Pyrogenes |
Salinem |
|
L. kirshneri |
Grippotyphosa |
Grippotyphosa |
Moska V |
|
L. interrogans |
Canicola |
Canicola |
Hond Utrecht IV |
|
L. interrogans |
Pomona |
Pomona |
Pomona |
|
L. interrogans |
Sejroe |
Wolffi |
3705 |
|
L. interrogans |
Sejroe |
Hardjo |
Hardjoprajitno |
|
L. borgpetersenii |
Tarassovi |
Tarassovi |
Perepelicin |
|
L. interrogans |
Australis |
Bratislava |
Jez-Bratislava |
|
*L. interrogans |
Sejroe |
Hardjo |
H-89 |
|
*L. interrogans |
Icterohaemorrhagie |
Icterohaemorrhagiae |
Palo Alto |
|
*L. interrogans |
Canicola |
Portland-vere |
Sinaloa ACR |
| http://www.pasteur.fr/recherche/Leptospira | * Aislados nacionales | ||
OBJETIVO.
La finalidad del presente trabajo fue realizar un seroperfil de leptospirosis utilizando la técnica de “MAT” en animales de dos unidades de producción caprina especializadas en producción lechera localizadas en el municipio de Apaseo el Alto, Guanajuato, con el objeto de conocer el estado inmune (anticuerpos) y sanitario de la población animal con respecto a esta enfermedad.

MATERIAL Y MÉTODOS.
Se trabajaron dos unidades de producción caprina especializadas en la producción de leche con antecedentes de trastornos reproductivos. Las unidades se localizan en el municipio de Apaseo el Alto, Guanajuato. Este se ubica en las coordenadas 100° 37′ 12″ de longitud oeste del Meridiano de Greenwich y en 20° 27′ 25″ de latitud norte. Posee una altitud de 1,853 m sobre el nivel del mar. Limita al norte con el municipio de Apaseo el Grande; al sur con el de Jerécuaro y Tarimoro; al oriente con el estado de Querétaro y al poniente con el municipio de Celaya, con una superficie de 375.09 km.
EVALUACIÓN DEL EVENTO.
La detección de anticuerpos contra Leptospira se realizó en el laboratorio de Leptospirosis del Centro Nacional de Investigaciones Disciplinarias en Microbiología Animal del Instituto Nacional de Investigaciones Forestales Agrícolas y Pecuarias en Palo Alto, México.
Se utilizó la prueba diagnóstica de Aglutinación microscópica “MAT” con antígeno vivo propuesta por la Organización Mundial de Sanidad Animal (OIE) y la Organización Mundial de la Salud (WHO) (Fig. 3).

Esta prueba se realizó con 12 diferentes serovariedades de Leptospira interrogans cultivadas en medio liquido (EMJH) libres de contaminación o auto-aglutinación (Cuadro 2). Nueve de referencia internacional, provenientes del Collaborating Centre for Reference and Research on Leptospirosis, Brisbane, Queensland, Australia, y tres serovariedades nacionales aisladas en la región norte y centro de México, tipificadas en el Departamento de Agricultura de Estados Unidos de Norteamérica “United States Department of Agriculture” (USDA) AMES IOWA (Dra. Carole A. Bolin DVM, PHD.).
Los sueros fueron trabajados en diluciones de 1:50 en adelante hasta dilución final, en placas serológicas de 96 pozos. Las reacciones fueron observadas al microscopio de campo oscuro a 160X. El título de corte fue la dilución mayor donde se observó el 50% de aglutinación o desaparición celular de Leptospiras del campo visual (Fig. 4).
MUESTREO.
Se realizó un muestreo en dos unidades caprinas productoras de leche. Las muestras sanguíneas se obtuvieron por punción de la vena yugular en un volumen de 5-7 ml con sistema vacuntainer (Fig. 5). En el laboratorio se centrifugaron los tubos a 1,500 – 2,000 rpm durante 5 a 10 minutos. El suero fue decantado en crioviales de 2 ml, que se identificaron individualmente con tinta indeleble y conservaron en congelación a –20oC hasta su utilización (Fig 6). Las muestras se tomaron de manera aleatoria y correspondieron a animales de diferentes edades 2, 3, 4, 5, 6 y 9 meses; 1, 2, 3 y 5 años así como sementales. De la unidad “A” con una población de 240 animales se tomaron 60 muestras que correspondió al 25% del total; de la unidad “B” de una población de 400 animales se muestrearon 134, que representó al 33.5% del total.

INSTALACIONES Y MANEJO.

Las instalaciones son de concreto, tabicón, herrería, pisos y corredor de cemento y techos de lámina. El agua proviene de pozo; algunos corrales tienen bebederos automáticos (Fig. 7) y otros adaptados de tambos de plástico (Fig. 8). Las unidades de producción están especializadas en la producción de leche, las razas muestreadas fueron Saanen, Nubia, Boer, Mancha y Alpina (Fig. 9). Su profilaxis sanitaria incluye calendarios de desparasitaciones y vacunas para diferentes enfermedades, pero ninguna contra leptospirosis. En ambas unidades de producción tienen perros y se reporta la presencia de roedores. No cuentan con un control de fauna nociva.
INTERPRETACIÓN DE ESTUDIOS SEROLÓGICOS.
Los criterios de evaluación fueron divididos en: a) Evento negativo o sueros sin reacción; b) Evento sospechoso: Sueros con títulos 1:50. c) Evento positivo: Sueros con títulos ≥ 1:100 (OIE, 2003; CDC, 1999). Títulos 1:100 a 1:200 fueron considerados positivos bajos, 1:400-1:800 positivos altos/moderados y de 1:1,600 en adelante positivos altos (Zamora, 1986; Herrera, 2007). De un total de 60 muestras de la unidad “A” el 68.3% (41/60) resultaron positivas, el 13.3% sospechosas y el 18.3% negativas (Gráfica 1). De un total de 134 muestras de la unidad “B” el 72.4% (97/134) resultaron positivas, el 10.4% sospechosas y el 17.2% negativas (Gráfica 2).


TÍTULOS
Los títulos de los animales de la unidad “A” oscilaron de 1:100 a 1:1,600 y fueron capaces de reaccionar hasta contra 5 diferentes serovariedades de L. interrogans (Cuadro 3 y 4). Los títulos de los sueros de la unidad “B” oscilaron de 1:100 a 1:800 y fueron capaces de reaccionar hasta contra 6 serovariedades (Cuadro 3 y 4).
|
Cuadro 3. Títulos de anticuerpos y frecuencias de la Unidad “A” y Unidad “B”. |
|||
|
TITULOS |
INTERPRETACIÓN |
FRECUENCIA UNIDAD “A” |
FRECUENCIA UNIDAD “B” |
|
1:100 |
Positivos/bajos |
51.3% |
65.6% |
|
1:200 |
Positivos /bajos |
28.2% |
16.4% |
|
1:400 |
Positivos altos/moderados |
17.9% |
16.9% |
|
1:800 |
Positivos altos /moderados |
1.3% |
1.1% |
|
1:1,600 |
Positivos altos |
1.3% |
0.0% |
|
Cuadro 4. Comparación de las frecuencias y títulos de anticuerpos Entre las unidades “A” y “B”. |
|||
|
TITULOS |
INTERPRETACIÓN |
Unidad “A” |
Unidad “B” |
|
1:100 a 1:200 |
Positivos/bajos |
79.5% |
82.0% |
|
1:400-1:800 |
Positivos altos /moderados |
19.2% |
18.0% |
|
1:1,600 |
Positivos altos |
1.3% |
0.0% |
Las frecuencias de los títulos reportadas por etapa etaria para la unidad “A” (Gráfica 3) y para la unidad “B” (Gráfica 4) variaron de un 20% (2-4 meses) a un 100% (adultos). Los animales fueron positivos con un 20% de frecuencia a partir de los 2 meses; a los 5-6 meses incrementaron su frecuencia de anticuerpos y de 9 meses a un año la frecuencia de animales positivos llega a un 100%; disminuye su frecuencia a los 2-3 años y vuelve a subir a los 5 años de edad. Los sementales tuvieron una frecuencia promedio del 54.5 al 90% (Cuadro 5).
|
Cuadro 5. Frecuencias y títulos de anticuerpos por etapa etaria. |
||||
|
EDAD |
Frecuencia Unidad “A” |
Títulos máximos Unidad “A” |
Frecuencia Unidad “B” |
Títulos máximos Unidad “B” |
|
2 meses |
s/d |
s/d |
20% |
1:800 |
|
3 meses |
s/d |
s/d |
70% |
1:400 |
|
4 Meses |
20% |
1:100 |
s/d |
s/d |
|
5 meses |
s/d |
s/d |
80% |
1:400 |
|
6 meses |
50% |
1:400 |
s/d |
s/d |
|
9 meses |
s/d |
s/d |
100% |
1:400 |
|
12 meses |
100% |
1:1600 |
s/d |
s/d |
|
2 años |
s/d |
s/d |
66% |
1:400 |
|
3 años |
50% |
1:200 |
s/d |
s/d |
|
5 años |
100% |
1:800 |
100% |
1:800 |
|
Sementales |
90% |
1:400 |
54.5 |
1:200 |
SEROVARIEDADES
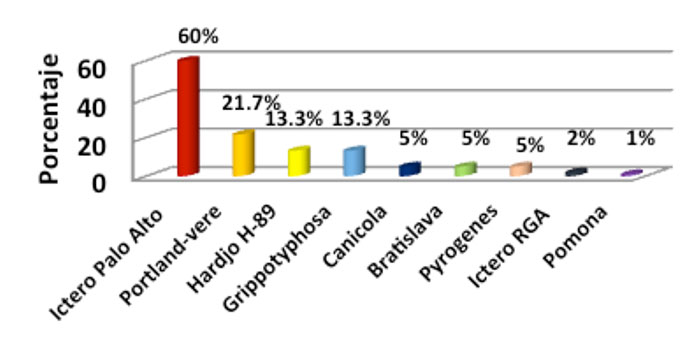
Las serovariedades más frecuentes en la unidad “A” fueron Icterohaemorrhagiae cepa Palo Alto (aislamiento), Canicola Portland-vere (aislamiento), Hardjo cepa H-89 (aislamiento), Grippotyphosa, Canicola Hond-Utrecht IV, Bratislava, Pyrogenes, Icterohaemorrhagiae cepa RGA y Pomona (Gráfica 5).
Las serovariedades más frecuentes en la unidad “B” fueron Bratislava, Icterohaemorrhagiae cepa Palo Alto (aislamiento), Canicola Hond Utrecht IV y Canicola serovariedad Portlandvere (aislamiento) (Gráfica 6).
|
Gráfica 3. Frecuencia de anticuerpos por etapa etaría. Unidad “A”. |
Gráfica 4. Frecuencia de anticuerpos por etapa etaria. Unidad “B” |
 |
 |
|
Gráfica 5. Porcentaje de animales con anticuerpos contra las diferentes serovariedades de Leptospira. Unidad “A”. |
Gráfica 6. Porcentaje de animales con anticuerpos contra las diferentes serovariedades de Leptospira. Unidad “B”. |
 |
 |

DISCUSIÓN Y CONCLUSIONES.
Se identificó la presencia de anticuerpos contra Leptospira spp en sueros provenientes de animales no vacunados de ambas unidades de producción. La frecuencia observada de animales positivos osciló de 68.3% a 70%, sospechosos de 13.3% a 10.4% y de negativos de 18.3% a 17.2%, se observó gran similitud en los resultados, en etapa etaria las frecuencias también fueron similares. Esta respuesta serológica nos permite inferir que la bacteria está afectando animales de ambos rebaños; lo cual podría deberse a la cercanía de instalaciones (menor a 1 km) así como al préstamo, manejo y compra venta de animales que se realiza entre las unidades de producción.
Con respecto a los títulos reportados, variaron de 1:100 a 1:1,600. Para la unidad “A” fueron 1:1,600 (altos) y para la “B” 1:800 (altos moderados) (Zamora, 1986; Herrera, 2007). Con respecto a las serovariedades, Icterohaemorrhagiae fue frecuente así como Canicola serovariedad Portlandvere, ambas asociadas a la presencia de ratas y perros respectivamente.

De acuerdo a la etapa etaria los anticuerpos anti leptospira se detectaron a partir de los dos meses de edad, periodo en que empieza a desaparecer la inmunidad pasiva proporcionada por el calostro de las hembras y los cabritos son más susceptibles a la infección. A partir de esta edad la frecuencia de anticuerpos contra leptospirosis se incrementa gradualmente, a los 3, 4, 5 y 6 meses hasta llegar a un 100% a los 9-12 meses, edad que coincide con el inicio de la etapa reproductiva de las hembras (primalas), donde la inmunosupresión debida a la gestación y la lactación provocan una mayor susceptibilidad a la infección (Tizard, 2002). Aquí es donde posiblemente algunos de los trastornos reproductivos como abortos y mortalidad perinatal puedan atribuirse a la leptospirosis. Los títulos tienden a estabilizarse en la edad media de los animales (2-3 años) y subir en la etapa madura (5 años) de las hembras a un 100% debido probablemente a continuos estímulos de la bacteria presente en el rebaño.
Es importante mencionar dentro de la epidemiología de la leptospirosis que la infección de uno sólo de los animales es suficiente para que sirva de “foco” de infección a los demás, ya que la bacteria tiende a diseminarse en el rebaño a través de la orina. Así mismo, hay que considerar que comúnmente las hembras tienden a parir en los corrales lo que ocasiona que placentas y secreciones vaginales entren en contacto con los demás animales de su rebaño. Se debe considerar que la orina, la leche y las descargas postparto son potenciales fuentes de infección por lo que los cabritos tienen altas posibilidades de infectarse y enfermarse en etapas tempranas ya que están expuestos a un medio propicio para contraer la enfermedad (Ellis et al. 1996).

Adicional a lo anteriormente mencionado las dos unidades cuentan con diversos factores de riesgo en su manejo, ejemplo: El traslado de cabritos del área de destete donde existen jaulas elevadas, bebederos automáticos y clima controlado (Fig. 10) a corrales de desarrollo con pisos de tierra, bebederos adaptados y sin cortinas (Fig. 11); por otra parte la falta de control de fauna nociva y el acceso de perros a las instalaciones también son factores que predisponen a la infección, ya que de acuerdo a esto, Peña (2012) reporta que en granjas con presencia de ratas, las cabras tienen 11 veces más posibilidades de ser positivas a leptospirosis y cuando existen perros, cuatro veces más. Finalmente se sugiere que en unidades de producción con trastornos reproductivos persistentes o que deseen mejorar la productividad, se implemente un programa de sanidad que involucre el diagnóstico y vacunación contra la leptospirosis. Es importante realizar una valoración de la situación reproductiva y productiva del rebaño antes y después del manejo, para poder evaluar el costo-beneficio de la vacunación.
CONCLUSIONES.
Se concluye que debido a no existir un programa de vacunación contra leptospirosis en las unidades de producción analizadas, los anticuerpos contra Leptospira spp detectados en el suero de los animales en estudio corresponden a un proceso infeccioso; y que al decidir vacunar, los productores tendrán como resultado: el control de la enfermedad, disminuir el riesgo de trasmisión de la infección hacía sus trabajadores y mejorar los parámetros reproductivos y productivos de sus rebaños en beneficio de su economía.
BIBLIOGRAFÍA.
Aborto ovino y caprino. http://www.vet-uy.com/articulos/ ovinos/050/006/ov006bas.htm
1.Hagan y Bruner. Enfermedades infecciosas de los animales domésticos. Cuarta Edición, La Prensa Médica Mexicana, S.A. 1981.
2.Hatem M.E. & Samir. The first recorded epidemic of leptospirosis in sheep in Egypt. Rev. sci. tech. Off. int. Epiz., 2014, 33 (3).
3.Herrera B. Leptospirosis interpretación de resultados serológicos en animales. 2007 www.produccion-animal.com.ar
4. Lilenbaum W., Morais ZM., Goncales AP., Souza GO., Richtzenhain L. and Vasconcellos SA. “First isolation of leptospires from dairy goats in Brazil. Braz. J. Microbiol. Vol.38 No. 3 Sao Paulo July/Sept. 2007.
5.Manual Merck de Veterinaria. Leptospirosis. Cuarta Edición. Ediciones Centrum Técnicas. Madrid, España 1988.
6.Morilla GA. Manual para el control de las enfermedades infecciosas de los cerdos. INIFAP-SAGAR y PAIEPEME, A.C. México, D.F., 1997.
7. Norma Oficial Mexicana NOM-029-SSA2-1999, Para la vigilancia epidemiológica, prevención y control de la leptospirosis en el humano. Estados Unidos Mexicanos – Secretaria de Salud 2012.
8. Norma Oficial Mexicana NOM-038-ZOO-1995, Requisitos mínimos para las bacterinas empleadas en la prevención y control de la leptospirosis bovina. Estados Unidos Mexicanos.- Secretaría de Agricultura, Ganadería y Desarrollo Rural. 9. Peña RJA. Estudio epidemiológico de la leptospirosis caprina en la zona centro del Estado de Veracruz. Tesis de Maestría. Facultad de Medicina Veterinaria y Zootecnia del Estado de Veracruz. Veracruz, Ver. Diciembre del 2012.
10. Santo BJA. Seroprevalencia y factores de riesgo asociados con la presencia de leptospirosis caprina en los municipios de Chiconquiaco, Coatepec, Coacoatzintla, Tlacolulan y Yecuatla, ubicados en la zona centro del Estado de Veracruz, México. Tesis de Licenciatura. Facultad de Medicina Veterinaria y Zootecnia del Estado de Veracruz. Veracruz, Ver. Julio 2010.
11.http://www.merckmanuals. com/vet /reproductive_ system/abortion_in_large_ animals/abortion_in_goats. html?qt= Leptospirosis& alt=sh
12. file:///C:/Users/INIFA/Documents/Lepto%20PR/leptospiro- sis%20Iowa.pdf
13. Zamora J. y Riedemann S. Consideraciones para la interpretación de la prueba de Aglutinación microscópica en el diagnóstico de la leptospirosis bovina. Arch. Med. Vet., Vol. XVIII No. 2, 1986.
14. Los principales abortos en la cabra. Leptospirosis [citado en 2014, Julio 30] Disponible de http://www.capraispana.com/ enfermedades/aborto/aborto.htm
15.World Health Organization. Zoonoses and veterinary public health. Leptospirosis. [cited on 2014, July 30]. Available from: http://www. who.int/zoonoses/diseases/leptospirosis/en/print.html.
16. World Health Organization. Human leptospirosis: guidance for diagnosis, surveillance and control. World Health Organization 2003. 17. World Health Organization-International Leptospirosis Society. Human leptospirosis: Guidance for diagnosis, surveillance and control. 2003. [cited on 2014 Aug 2]. Available from: http://www.leptonet.net/assets/images/LeptoGuidelines_Print_version_19May03.pdf
Artículo publicado en Entorno Ganadero










