RAMÍREZ SALINAS GRACIELA
Departamento de Medicina y Zootecnia de Aves
MÉNDEZ BERNAL ADRIANA
Departamento de Patología FMVZ-UNAM. Patólogo Veterinario. Responsable de Diagnóstico. Depto. Aves FMVZ-UNAM.
SÁNCHEZ GODOY FÉLIX
Departamento de Medicina y Zootecnia de Aves,
[email protected]
INTRODUCCIÓN
La clamidiosis aviar es una enfermedad infecciosa aguda o crónica de las aves silvestres y domésticas, producida por una bacteria cocoide Gram (-), conocida como Chlamydia psittaci, es un microorganismo intracelular obligado, posee ADN y ARN, y es capaz de sintetizar sus propios sistemas enzimáticos (Martínez y Tinetti, 2007).
El ciclo consiste en cinco fases: 1) adherencia y penetración por el cuerpo elemental (CE), 2) transición del CE metabólicamente inerte al cuerpo reticular (CR) metabólicamente activo, 3) multiplicación del CR mediante fisión binaria, progenie, 4) maduración de los CR no infecciosos a CE infecciosos, y 5) liberación de CE de las células huésped (Swayne, 2013.). La C. psittaci puede transmitirse en las aves por inhalación de polvo o partículas infecciosas en el aire, y por la ingestión de material infeccioso.

FIGURA 1. Clamidiosis. Cadáveres de cuatro loros Amazonas que muestran buena condición corporal y del plumaje.
El presente trabajo tiene por objetivo describir las lesiones macro y microscópicas más frecuentes en psitácidos afectados por C. psittaci a partir de muestras de cadáveres y órganos de trece psitácidos de diferentes géneros, los cuales fueron remitidos durante el 2015 al Laboratorio de Diagnóstico e Investigación en Enfermedades de las Aves del Departamento de Medicina y Zootecnia de Aves de la Facultad de Medicina Veterinaria y Zootecnia de la Universidad Nacional Autónoma de México.
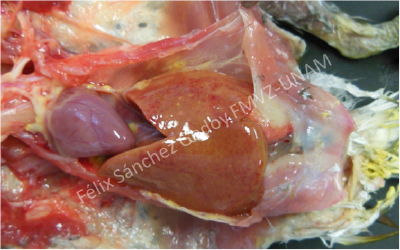
FIGURA 2. Clamidiosis. Cadáver de un loro Amazonas en donde se observa aerosaculitis fibrinosa y hepatitis necrótica multifocal.
DESCRIPCIÓN DE LOS CASOS
Historia clínica
CASO 1
En enero de 2015 se presentó un episodio de mortalidad en psitácidos de los géneros Ara y Amazona alojadas en un aviario localizado en el Estado de México que funciona como Unidad de Manejo para la Conservación de la Vida Silvestre (UMA). El alojamiento de las aves consiste en un encierro al aire libre cuyas dimensiones van de 60 m largo x 10 m profundidad x 3 m altura, con vegetación natural, donde convivían 35 aves en total; 19 de las cuales eran Psitaciformes de los géneros Ara, Amazona y Aratinga. La mayoría de las aves presentaron anorexia, letargia y plumas erizadas, así como diarrea y secreción nasal. En total, murieron 11 aves adultas (57%) de las cuales 7 aves fueron enviadas al Laboratorio de Diagnóstico donde se realizó necropsia e histopatología en dos loros tamaulipecos (Amazona viridigenalis), un loro cabeza amarilla (Amazona oratrix), un loro nuca amarilla (Amazona auropalliata), un loro mejillas amarillas (Amazona autumnalis) y dos guacamayas verdes (Ara militaris) (Figura 1).
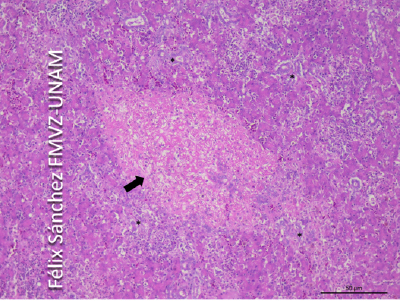
FIGURA 3. Clamidiosis. Fotomicrografía de hígado en donde se observa extensas zonas de necrosis coagulativa de hepatocitos (flecha), proliferación de conductos biliares (asteriscos) y agregados de células inflamatorias. Tinción H&E, Barra 50 μm.
CASO 2
Se reciben muestras de órganos en formol de aves provenientes del Centro para la Conservación e Investigación de la Vida Silvestre (CIVS) ubicado en el Estado de Jalisco. Se trata de un loro corona lila (Amazona finschi) y tres pericos atoleros (Aratinga canicularis). Los signos generales que presentaban son: diarrea amarilla, poliuria, polidipsia, depresión y plumaje erizado. Su dieta consistía en cítricos, pepino, mango, papaya y semillas de girasol.
CASO 3
Se reciben los cadáveres de dos psitácidos provenientes de un aviario del Estado de México que funciona como Unidad de Manejo para la Conservación de la Vida Silvestre (UMA). Se han documentado 12 psitácidos muertos de forma súbita de los cuales se envían dos ejemplares: un loro cabeza de viejito (Pionus senilis) y un loro mejillas amarillas (Amazona autumnalis), no hay datos sobre los signos clínicos, dieta y alojamiento de las aves.
GRÁFICA 1. Lesiones macroscópicas causadas por Chlamydia psittaci en aves de México
Hallazgos macroscópicos
CASO 1
Las lesiones macroscópicas más sobresalientes fueron aerosaculitis fibrinosa de moderada a severa (7/7), proventriculitis catarral moderada difusa (4/7), hepatitis necrótica moderada multifocal (3/7), hepatomegalia moderada (3/7), hemorragias multifocales en encéfalo (2/1), mientras que pericarditis fibrinosa grave difusa, esplenitis necrótica moderada y atrofia moderada del bazo sólo se presentaron en un ave.
CASO 2
En este caso sólo se enviaron los órganos fijados en formol.
CASO 3
Las principales lesiones a la necropsia fueron hepatitis necrótica grave multifocal coalescente aguda (2/2), aerosaculitis fibrinosa moderada difusa aguda (2/2) y hemorragias multifocales en corazón (1/2) (Figura 2).
La frecuencia de lesiones macroscópicas de los tres casos se encuentra descrita en la Gráfica 1.
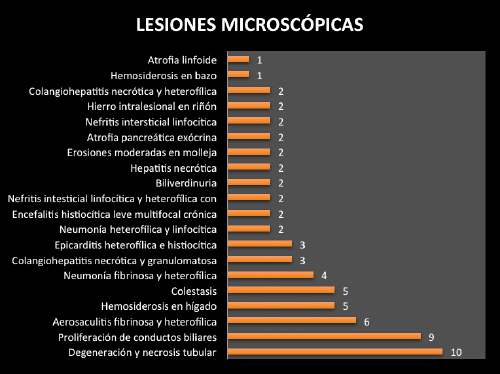
GRÁFICA 2. Lesiones microscópicas causadas por Chlamydia psittaci en aves de México
Hallazgos microscópicos
CASO 1
Las principales lesiones microscópicas fueron: Colangiohepatitis necrótica y heterofílica grave multifocal coalescente aguda a subaguda con proliferación de conductos biliares, colestasis y hierro (2/6), aerosaculitis fibrinosa y heterofílica grave difusa aguda (6/6), degeneración y necrosis tubular aguda moderada multifocal con bilis y hierro intralesional, degeneración y necrosis tubular aguda moderada multifocal (6/6) con bilis y hierro intralesional (2/6), atrofia linfoide moderada difusa (1/6), epicarditis heterofílica e histiocítica moderada zonalmente extensiva (3/6) y neumonía fibrinosa y heterofílica moderada multifocal coalescente (4/6).
Las principales lesiones fueron: Colangiohepatitis necrótica y granulomatosa grave multifocal coalescente crónica-activa con proliferación de conductos biliares, colestasis y hierro (3/4), nefritis intersticial linfocítica moderada multifocal subaguda (2/4), y atrofia pancreática exócrina (2/4), erosiones moderadas en molleja (2/4) y hemosiderosis moderada difusa en bazo (1/4).
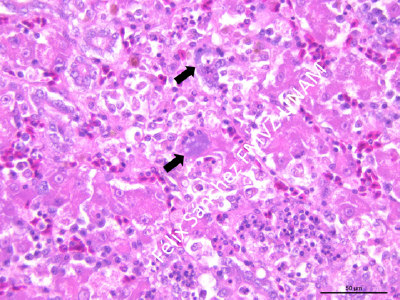
FIGURA 4.Clamidiosis. Fotomicrografía de hígado, en el citoplasma de hepatocitos y de las células epiteliales de los conductos biliares se observan colonias bacterias cocoides basofílicas (células manchadas) (flechas). También se observa proliferación de conductos biliares e inflamación. Tinción H&E, Barra 50 μm.
CASO 3
Las principales lesiones microscópicas fueron: Hepatitis necrótica grave multifocal coalescente aguda con proliferación e hiperplasia de conductos biliares (2/2) (Figura 3), aerosaculitis fibrinosa grave difusa aguda (2/2), Nefritis intersticial linfocítica y heterofílica moderada multifocal con trombos intraglomerulares y, degeneración y necrosis tubular aguda moderada (2/2), encefalitis histiocítica leve multifocal crónica (2/2) y neumonía heterofílica y linfocítica moderada multifocal aguda.
La frecuencia de lesiones microscópicas de los tres casos se encuentra descrita en la gráfica 2.
Pruebas de histoquímica
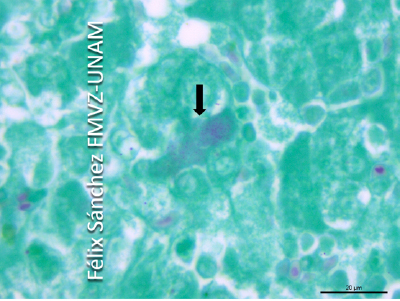
Con la tinción de rutina de hematoxilina y eosina, en la mayoría de los cortes de hígado de los tres casos, se observaron colonias bacterianas cocoides ligeramente basofílicas, menores a 1 μm de diámetro intracitoplasmáticas (inclusión clamidial) en hepatocitos, células epiteliales y macrófagos (células manchadas) (Figura 4) que se tiñen de color rojo-púrpura con la tinción especial de Giménez (Figura 5) y de color azul- púrpura con la tinción especial de Giemsa (Figura 6). Así mismo, se realizó la tinción de Gram y no se apreciaron colonias bacterianas. En los cortes examinados de los sacos aéreos de los tres casos no fueron observados las colonias bacterianas cocoides intracelulares.
FIGURA 5. Fotomicrografía de hígado, el citoplasma de un hepatocito contiene colonias bacterianas cocoides que se tiñen de color rojo- púrpura (flecha). Tinción de Giménez, Barra 20 μm.
Pruebas complementarias
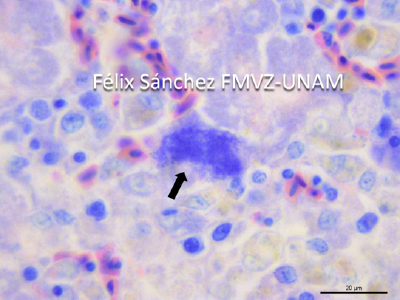
FIGURA 6.Clamidiosis. Fotomicrografía de hígado, el citoplasma de un hepatocito contiene colonias bacterianas cocoides que se tiñen de color azul-púrpura (flecha). Tinción de Giemsa, Barra 20 μm.
Criterios diagnósticos
Las lesiones a la necropsia y microscópicas, aunadas a las pruebas histoquímica de Giménez y Giemsa, complementadas con la microscopía electrónica, demuestran que la causa de enfermedad y muerte de los psitácidos de los tres casos se encuentra asociada a Chlamydia sp
Diagnósticos diferenciales
Los diagnósticos diferenciales principalmente incluyen agentes infecciosos que ocasionan muerte súbita asociada a daño hepático como la enfermedad de Pacheco que se encuentra asociada a un Herpesvirus, que se caracteriza por ocasionar necrosis hepática multifocal y cuerpos de inclusión intranucleares eosinofílico con formación de sincitios, así mismo, otros agentes infecciosos capaces de inducir hepatitis necrótica son los Adenovirus y los Poliomavirus en donde se aprecian cuerpos de inclusión intranucleares basofílicos y eosinofílicos, y cuerpos de inclusión intranucleares anfofilicos con cariomegalia respectivamente.
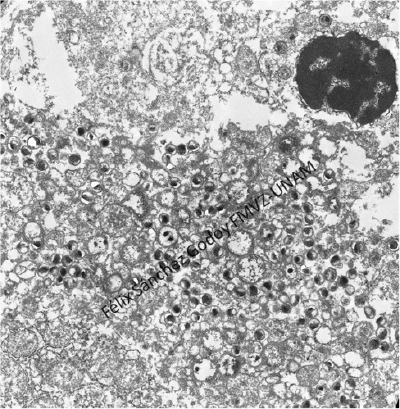
FIGURA 7. Clamidiosis. Microfotografía electrónica de transmisión de un hepatocito, en el citoplasma se aprecian vacuolas electrolúcidas que contienen estructuras redondas compatibles con cuerpos elementales y reticulares de Chlamydia.
DISCUSIÓN
Las principales lesiones macroscópicas detectas en la necropsia del caso 1 y 3 fueron hepatitis necrótica, aerosaculitis fibrinosa, pericarditis fibrinosa y esplenitis necrótica, estas lesiones coinciden con las reportadas por Ecco et al en el 2009, en donde describe un brote de Clamidiosis en 15 aves, 13 loros Amazonas (Amazona aestiva), un Aratinga aurea y un Pionus maximiliani, decomisados del comercio ilegal en Brasil, las 15 aves presentaron hepatomegalia con focos de necrosis multifocales, 10 de las aves mostraron aerosaculitis fibrinosa y siete con esplenomegalia. Freitas Raso et al en el 2004 describen otro brote de Clamidiosis en 58 polluelos de loros amazonas, de 1-2 meses de edad, (A. aestiva), recuperados del comercio ilegal. Reportan una mortalidad del 96.5% y sólo a 10 aves se les realizaron estudios post mortem. Macroscópicamente se observó hepatomegalia (10/10) y focos de necrosis (5/10). La literatura reporta que uno de los hallazgos macroscópicos comunes en aves con Clamidiosis son hepatomegalia, esplenomegalia y aerosaculitis; el hígado de las aves afectadas presenta aumento de tamaño, coloración café claro y abundante cantidad de focos de necrosis de color gris – amarillo tal como se observó en las aves remitidas al laboratorio (Schmidt, 2008.)
La presencia de hemorragias y fibrina en diferentes órganos puede estar asociada a un posible daño vascular, mediante inmunohistoquímica se ha demostrado la presencia de C. psittaci en las células endoteliales por lo que se puede inferir un daño vascular por la multiplicación y la producción de toxinas por parte de la bacteria (van Buuren et al., 1994).
Las lesiones microscópicas principalmente se localizaron en hígado, sacos aéreos, riñón y bazo. En la mayoría de los casos se detectó colangiohepatitis cuya lesión principal varia ba de necrótica a granulomatosa dependiendo del curso de la enfermedad, así mismo se apreció proliferación de conductos biliares y colestasis en la mayoría de los cortes histopatológicos. Esto difiere con lo reportado en la literatura por Ecco et al en el 2009 y Freitas Raso et al en el 2004 en donde describen que la mayoría de los hígados afectados por C. psittaci presentaron infiltrado inflamatorio linfoplasmocítico con necrosis hepatocelular multifocal, así como hepatitis granulomatosa y proliferación de conductos biliares. En estos dos estudios no se describe la afectación de los conductos biliares a diferencia de este trabajo en donde se reporta en cinco ocasiones, esto se puede deber a que la cepa de C. psittaci presente en México quizá tenga un mayor tropismo por las células epiteliales que por lo macrófagos, este comentario se apoya en que la presencia de inclusiones clamidiales fue más frecuente en las células epiteliales de los conductos biliares y los hepatocitos que en los macrófagos, lo que difiere en la literatura en donde describen las bacterias principalmente en los macrófagos del hígado (Freitas et al., 2004).
La presencia de hierro en hígado, bazo y riñón es considerada como hemosiderosis y generalmente se asocia a un exceso de hierro en la dieta. La degeneración y la necrosis tubular aguda son consideradas secundarias al choque séptico que presentaban las aves. Así mismo, la aerosaculitis, neumonía, epicarditis, nefritis y encefalitis están asociadas al proceso bacteriano sistémico (Knittler y Sachse, 2015).
En la mayoría de los cortes de hígado se observaron colonias bacterianas cocoides (inclusiones clamidiales) ligeramente basofílicas, menores a 1 μm de diámetro intracitoplasmáticas en hepatocitos, células epiteliales y macrófagos (células manchadas) que se tiñen de color rojo con la tinción especial de Giménez y de color morado a azul con la tinción especial de Giemsa. En la literatura consultada se menciona que las inclusiones clamidiales raramente son observadas en los cortes histopatológicos y generalmente se encuentran en el citoplasma de los macrófagos del hígado y el bazo, esta diferencia se podría deber a que la mayoría de las aves se encontraron en un curso agudo de la enfermedad en donde hay una mayor cantidad de bacterias, así mismo, se puede mencionar que las inclusiones clamidiales se detectan con mayor facilidad con la tinción especial de Giemsa en las células epiteliales de los conductos biliares
CONCLUSIÓN
Las lesiones macro y microscópicas asociadas a C. psittaci pueden variar de acuerdo al huésped, virulencia de la cepa, edad de las aves, factores predisponentes y complicantes, sin embargo, de acuerdo a las lesiones reportadas en este estudio aunado a la revisión de la literatura se puede mencionar que el encontrar lesiones en psitácidos neotropicales, de hepatitis necrótica, aerosaculitis fibrinosa, y esplenomegalia, e histológicamente colangiohepatitis necrótica a granulomatosa, con proliferación de conductos biliares y colestasis, asociado a bacterias cocoides intracelulares (inclusiones clamidiales), Giemsa o Giménez positivas son indicativas de Clamidiosis.
Agradecimientos
Los autores agradecen al histotecnólogo Alfredo Díaz Estrada por su colaboración en el proceso histológico y las tinciones especiales.
BIBLIOGRAFÍA
1. College of Veterinary Medicine. Psitacosis / Clamidiosis aviar. 2009.
2. Ecco R, Preis IS, Martins NRS, Vilela DAR, Shivaprasad HL. 2009. An outbreak of chlamydiosis in captive psittacines. Brazilian Journal of Veterinary Pathology. 2 (2): 85-90.
3. Freitas RT, Nery GS, Milanelo L, Almeida IC, Reiko ME, Pessoa AJ, and Augusto PA. 2004. An Outbreak of Chlamydiosis in Captive Blue- Fronted Amazon Parrots (Amazona aestiva) in Brazil. Journal of Zoo and Wildlife Medicine. 35 (1):94-96.
4. Katoh H, Ogawa H, Ohya K, Fukushi H. 2010. A Review of DNA Viral Infections in Psittacine Birds. J Vet Med Sci. 72(9):1099-106.
5. Martínez KP, Tinetti PS. 2007. Determinación de anticuerpos contra Chlamydophila psittaci por prueba de ELISA en aves psitácidas tropicales mantenidas en cautiverio en el área metropolitana de San Salvador. Universidad de el Salvador. Facultad de Ciencias Agronómicas. Departamento de Medicina Veterinaria.
6. Knittler MR and Sachse K. 2015. Chlamydia psittaci: update on an underestimated zoonotic agent. Pathoq Dis. 73 (1):1-15.
7. OIE, Clamidiosis aviar. Manual terrestre, 2012. [Citado el 05 de marzo de 2016].
8. Schmidt RE, Reavill DR, Phalen DN. 2008. Pathology of Pet and Aviary Birds. Ames, Iowa: Iowa State Press.
9. Swayne DE. 2013. Diseases of Poultry. 13th Edition. Department of Agriculture. Athens, Georgia. United States. 1055 – 1068.
10. van Buuren CE, Dorrestein GM, van Dijk JE. 1994. Chlamydia psittaci infections in birds: A review on the pathogenesis and histopathological features. Vet Q. 16 (1):38-41.
11. Zachary JF, McGavin MD. 2012. Pathologic Basis of Veterinary Disease. 5th Edition. Elsevier Health Sciences. St Louis, Misouri, United States.
Artículo publicado en Los Avicultores y su Entorno Abril-Mayo 2017